《腹腔內(nèi)窺鏡手術(shù)系統(tǒng)技術(shù)審查指導(dǎo)原則 第1部分:手術(shù)器械(征求意見(jiàn)稿)》旨在指導(dǎo)醫(yī)療器械注冊(cè)?申請(qǐng)人對(duì)腹腔內(nèi)窺鏡手術(shù)系統(tǒng)用不向患者提供能量的手術(shù)器械和高頻手術(shù)器械(以下簡(jiǎn)稱(chēng)手術(shù)器械)注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫(xiě)�,同時(shí)也為技術(shù)審評(píng)部門(mén)審查注冊(cè)申報(bào)資料提供參考。
腹腔內(nèi)窺鏡手術(shù)系統(tǒng)技術(shù)審查指導(dǎo)原則 第1部分:手術(shù)器械
(征求意見(jiàn)稿)
本指導(dǎo)原則旨在指導(dǎo)醫(yī)療器械注冊(cè)申請(qǐng)人對(duì)腹腔內(nèi)窺鏡手術(shù)系統(tǒng)用不向患者提供能量的手術(shù)器械和高頻手術(shù)器械(以下簡(jiǎn)稱(chēng)手術(shù)器械)注冊(cè)申報(bào)資料的準(zhǔn)備及撰寫(xiě)�����,同時(shí)也為技術(shù)審評(píng)部門(mén)審查注冊(cè)申報(bào)資料提供參考。
本指導(dǎo)原則是對(duì)手術(shù)器械的一般要求���,申請(qǐng)人應(yīng)依據(jù)產(chǎn)品的具體特性確定其中內(nèi)容是否適用��。若不適用��,需具體闡述理由及相應(yīng)的科學(xué)依據(jù)����,并依據(jù)產(chǎn)品的具體特性對(duì)注冊(cè)申報(bào)資料的內(nèi)容進(jìn)行充實(shí)和細(xì)化�。
本指導(dǎo)原則是供注冊(cè)申請(qǐng)人和技術(shù)審評(píng)人員使用的指導(dǎo)性文件,但不包括審評(píng)審批所涉及的行政事項(xiàng)�,亦不作為法規(guī)強(qiáng)制執(zhí)行,應(yīng)在遵循相關(guān)法規(guī)的前提下使用本指導(dǎo)原則���。如果有能夠滿足相關(guān)法規(guī)要求的其他方法��,也可以采用�,但是需要提供詳細(xì)的研究資料和驗(yàn)證資料����。
本指導(dǎo)原則是在現(xiàn)行法規(guī)和標(biāo)準(zhǔn)體系以及當(dāng)前認(rèn)知水平下制定,隨著法規(guī)和標(biāo)準(zhǔn)的不斷完善,以及科學(xué)技術(shù)的不斷發(fā)展��,相關(guān)內(nèi)容也將適時(shí)進(jìn)行調(diào)整��。
一�����、適用范圍
本指導(dǎo)原則中的手術(shù)器械是腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的末端執(zhí)行器�,安裝在機(jī)械臂上用于執(zhí)行手術(shù)任務(wù)�。本指導(dǎo)原則所覆蓋手術(shù)器械包括不向患者提供能量的手術(shù)器械和高頻手術(shù)器械。不包括單孔腹腔內(nèi)窺鏡手術(shù)系統(tǒng)用手術(shù)器械���。其他手術(shù)器械可參考本指導(dǎo)原則的適用部分����。
二���、注冊(cè)審查要點(diǎn)
(一)監(jiān)管信息
1.產(chǎn)品名稱(chēng)
產(chǎn)品名稱(chēng)應(yīng)符合《醫(yī)療器械通用名稱(chēng)命名規(guī)則》和國(guó)家標(biāo)準(zhǔn)���、行業(yè)標(biāo)準(zhǔn)、規(guī)范性文件中的通用名稱(chēng)要求�。產(chǎn)品名稱(chēng)由一個(gè)核心詞和不超過(guò)三個(gè)的特征詞組成。手術(shù)器械可作為腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的產(chǎn)品組成進(jìn)行注冊(cè),也可單獨(dú)進(jìn)行注冊(cè)�����。作為腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的產(chǎn)品組成進(jìn)行注冊(cè)時(shí)���,產(chǎn)品名稱(chēng)體現(xiàn)在內(nèi)窺鏡手術(shù)系統(tǒng)的結(jié)構(gòu)組成中��,建議為“特征詞+器械類(lèi)型”�,特征詞可體現(xiàn)產(chǎn)品結(jié)構(gòu)特點(diǎn)��、功能���、工作原理等�,器械類(lèi)型可以為鉗�����、剪�、鑷等,如持針鉗����、單極弧剪���、雙極彎型抓鉗等;單獨(dú)注冊(cè)時(shí)���,產(chǎn)品名稱(chēng)建議為“腹腔內(nèi)窺鏡手術(shù)系統(tǒng)用手術(shù)器械”或“腹腔內(nèi)窺鏡手術(shù)系統(tǒng)用高頻手術(shù)器械”�����。
2.注冊(cè)單元?jiǎng)澐?/span>
注冊(cè)單元?jiǎng)澐謶?yīng)符合《醫(yī)療器械注冊(cè)單元?jiǎng)澐种笇?dǎo)原則》的要求�,原則上以產(chǎn)品的技術(shù)原理����、結(jié)構(gòu)組成�、性能指標(biāo)和適用范圍為劃分依據(jù)。
單獨(dú)注冊(cè)時(shí)��,高頻手術(shù)器械和不向患者提供能量的手術(shù)器械原則上劃分為不同的注冊(cè)單元�����;高頻手術(shù)器械中的單極器械和雙極器械可作為一個(gè)注冊(cè)單元�����。高頻手術(shù)器械配合使用的通用高頻手術(shù)設(shè)備及其附件(如中性電極、腳踏開(kāi)關(guān)等)一般不與手術(shù)器械一起注冊(cè)�。
(二)綜述資料
1.概述
申請(qǐng)人需描述手術(shù)器械的通用名稱(chēng)及確定依據(jù)、適用范圍���。如適用���,申請(qǐng)人應(yīng)提供手術(shù)器械的背景信息概述。
2.產(chǎn)品描述
2.1工作原理
應(yīng)描述手術(shù)器械的工作原理����。
應(yīng)提供醫(yī)生控制臺(tái)到手術(shù)器械的控制原理圖,說(shuō)明醫(yī)生控制臺(tái)如何實(shí)現(xiàn)對(duì)手術(shù)器械的控制��。提供醫(yī)生控制臺(tái)與手術(shù)器械末端的運(yùn)動(dòng)比例�����,如比例可調(diào)�����,應(yīng)說(shuō)明運(yùn)動(dòng)比例的調(diào)節(jié)范圍�、調(diào)節(jié)或切換方式。
手術(shù)器械用于傳輸動(dòng)力�����、實(shí)現(xiàn)器械控制的方式有絲傳動(dòng)、齒輪傳動(dòng)和桿傳動(dòng)等�,通常采用絲傳動(dòng)和齒輪傳動(dòng)相結(jié)合的方式。應(yīng)說(shuō)明器械盒部分的動(dòng)力傳輸至器械末端的方式�����。
說(shuō)明手術(shù)器械實(shí)現(xiàn)的自由度數(shù)量��、各自由度的運(yùn)動(dòng)方向����、運(yùn)動(dòng)范圍和實(shí)現(xiàn)方式,并提供各自由度的圖示����。如自由度的實(shí)現(xiàn)需要器械臂的配合應(yīng)給出說(shuō)明并提供圖示����。
2.2 結(jié)構(gòu)組成
手術(shù)器械一般由器械盒、器械桿和器械末端組成(如圖1)�。高頻手術(shù)器械的器械盒帶有高頻連接線接口,用于連接高頻手術(shù)設(shè)備��。
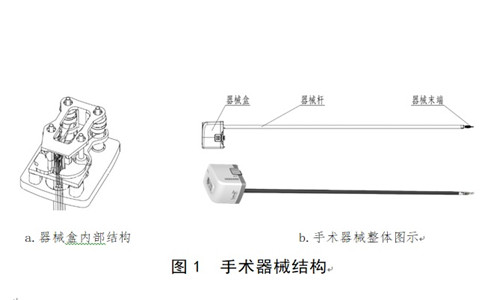
應(yīng)提供手術(shù)器械整體圖示及細(xì)節(jié)圖示,如器械盒�、器械桿、器械末端等��。
說(shuō)明手術(shù)器械如何與器械臂接口連接���,提供連接方法說(shuō)明及連接接口的細(xì)節(jié)圖����。說(shuō)明手術(shù)器械與器械臂的對(duì)應(yīng)關(guān)系����,可以各器械臂互換還是僅限于某一器械臂。
通過(guò)高頻電纜連接高頻手術(shù)設(shè)備的能量接口和器械盒中的接口���,用于將高頻能量傳輸至高頻手術(shù)器械�����。應(yīng)說(shuō)明高頻手術(shù)器械如何與高頻手術(shù)設(shè)備連接�����,提供接口圖示(與高頻手術(shù)設(shè)備接口���、與機(jī)械臂接口)�����。如高頻電纜作為產(chǎn)品組成��,應(yīng)提供長(zhǎng)度等信息�。
高頻手術(shù)器械如配合專(zhuān)用高頻手術(shù)設(shè)備工作����,應(yīng)提供該設(shè)備的制造商、型號(hào)�。
與單極手術(shù)器械配合使用的中性電極如有要求應(yīng)說(shuō)明。高頻手術(shù)器械末端如需配合能量護(hù)套使用����,應(yīng)提供能量護(hù)套的相關(guān)信息,如材質(zhì)����、使用方式��、是否無(wú)菌提供等��,并提供能量護(hù)套的圖示及配合手術(shù)器械后的圖示。
2.3 主要功能
高頻手術(shù)器械可分為單極手術(shù)器械(如圖2)和雙極手術(shù)器械(如圖3)��,單極手術(shù)器械如單極剪刀����、單極電鉤等,一般用于分離����、切割及凝血;雙極手術(shù)器械如雙極鉗��、雙極鑷等�,一般用于組織剝離、凝血�����。

不向患者提供能量的手術(shù)器械(如圖4)按其功能通常分為持針鉗類(lèi)��、剪類(lèi)����、抓持器類(lèi)、施夾鉗類(lèi)等。持針鉗類(lèi)器械一般用于實(shí)現(xiàn)夾持�、縫合、打結(jié)等操作���。剪類(lèi)器械一般用于實(shí)現(xiàn)剪線���、解剖、切割等操作���。抓持器類(lèi)器械一般用于實(shí)現(xiàn)抓持����、牽拉等操作����,可分為有創(chuàng)抓持和無(wú)創(chuàng)抓持,如鑷�、抓持器、牽開(kāi)器等����。施夾鉗類(lèi)器械一般用于配合結(jié)扎夾進(jìn)行結(jié)扎。

應(yīng)描述手術(shù)器械的主要功能及其組成部件(如器械盒����、器械桿和器械末端)的功能。
應(yīng)提供為實(shí)現(xiàn)手術(shù)器械的預(yù)期用途而配合使用的附件(如能量護(hù)套)信息���。
2.4型號(hào)規(guī)格
對(duì)于存在多種型號(hào)規(guī)格的手術(shù)器械�,應(yīng)列表說(shuō)明各型號(hào)規(guī)格的區(qū)別�����,提供不同型號(hào)規(guī)格的功能���、配合使用的設(shè)備���、提供方式、使用次數(shù)等信息��。對(duì)于高頻手術(shù)器械����,應(yīng)明確為單極還是雙極。手術(shù)器械描述如表1所示���。
表1 手術(shù)器械列表舉例
器械 名稱(chēng) | 規(guī)格型號(hào) | 提供 方式 | 貨架壽命/使用次數(shù) | 功能 描述 | 頭端 圖示 |
持針鉗 | **** | 非無(wú)菌 | 10次 | 用于持針進(jìn)行縫合�����。 |
|
2.5包裝說(shuō)明
應(yīng)說(shuō)明手術(shù)器械的包裝信息��,如包裝材料�����、用途等���,如有多層包裝應(yīng)分別提供�����,并提供各層包裝的圖示���。
對(duì)于無(wú)菌提供的手術(shù)器械,應(yīng)提供無(wú)菌屏障系統(tǒng)的信息����,如材質(zhì)等,還應(yīng)說(shuō)明如何確保最終使用者可清晰的辨識(shí)包裝的完整性�。
若使用者在進(jìn)行滅菌前需要包裝手術(shù)器械或附件時(shí),應(yīng)當(dāng)提供正確包裝的信息(如材料�����、成分和尺寸等)。
2.6研發(fā)歷程
如適用�,應(yīng)描述申報(bào)產(chǎn)品的研發(fā)背景和目的����,如申報(bào)產(chǎn)品的研發(fā)歷史概述、歷次注冊(cè)申請(qǐng)?zhí)峤坏男畔?���。此外,還應(yīng)在研發(fā)背景中描述產(chǎn)品改進(jìn)的內(nèi)容��、實(shí)現(xiàn)方式����、意義、解決的技術(shù)問(wèn)題或臨床問(wèn)題等��。
2.7與同類(lèi)和/或前代產(chǎn)品的參考和比較
對(duì)于研發(fā)參考的同類(lèi)產(chǎn)品或前代產(chǎn)品����,應(yīng)說(shuō)明選擇其作為研發(fā)參考的原因。同時(shí)列表說(shuō)明申報(bào)產(chǎn)品與研發(fā)參考產(chǎn)品在工作原理����、結(jié)構(gòu)組成�����、性能指標(biāo)及適用范圍等方面的異同�����。
區(qū)別于其他同類(lèi)產(chǎn)品的特征是技術(shù)審評(píng)的關(guān)注點(diǎn)���,如手術(shù)器械適用范圍、結(jié)構(gòu)組成����、性能指標(biāo)等。
3. 適用范圍
申請(qǐng)人應(yīng)依據(jù)臨床評(píng)價(jià)資料并結(jié)合相關(guān)臨床診療規(guī)范來(lái)確定產(chǎn)品的適用范圍����。
單獨(dú)申報(bào)的手術(shù)器械,適用范圍應(yīng)明確配合使用腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的注冊(cè)人和規(guī)格型號(hào)��,如“本產(chǎn)品與***(注冊(cè)人名稱(chēng))生產(chǎn)的型號(hào)為***的腹腔內(nèi)窺鏡手術(shù)系統(tǒng)配合使用����?!笔中g(shù)器械的功能在產(chǎn)品技術(shù)要求的規(guī)格型號(hào)列表中體現(xiàn),參考表1��。
4. 申報(bào)產(chǎn)品上市歷史
如適用���,申請(qǐng)人需提供以下相關(guān)資料:
4.1 上市情況��。申報(bào)產(chǎn)品在各國(guó)家或地區(qū)的上市批準(zhǔn)時(shí)間、銷(xiāo)售情況�。
4.2 不良事件和召回。
4.3銷(xiāo)售�����、不良事件及召回率����。
(三)非臨床資料
1. 產(chǎn)品風(fēng)險(xiǎn)管理資料
內(nèi)窺鏡手術(shù)系統(tǒng)用手術(shù)器械的風(fēng)險(xiǎn)管理報(bào)告應(yīng)符合YY/T 0316《醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用》的有關(guān)要求,審查要點(diǎn)包括:
1.1與產(chǎn)品有關(guān)的安全性特征判定可參考YY/T 0316的附錄C����。附錄C的清單是不詳盡的,確定產(chǎn)品安全性特征應(yīng)具有合理的可預(yù)見(jiàn)性�����,應(yīng)當(dāng)仔細(xì)考慮“會(huì)在什么時(shí)候、在哪兒�、出現(xiàn)什么問(wèn)題”。
1.2危害��、可預(yù)見(jiàn)的事件序列和危害處境判斷可參考YY/T 0316附錄E�、I;
1.3風(fēng)險(xiǎn)控制的方案與實(shí)施�����、綜合剩余風(fēng)險(xiǎn)的可接受性評(píng)價(jià)及生產(chǎn)和生產(chǎn)后監(jiān)視相關(guān)方法可參考YY/T 0316附錄F�����、G�、J;
1.4風(fēng)險(xiǎn)可接受準(zhǔn)則�,降低風(fēng)險(xiǎn)的措施及采取措施后風(fēng)險(xiǎn)的可接收程度,是否有新的風(fēng)險(xiǎn)產(chǎn)生�����。應(yīng)提供采取風(fēng)險(xiǎn)控制措施前后的風(fēng)險(xiǎn)矩陣表����,有綜合剩余風(fēng)險(xiǎn)是否可接受的判定���。
附錄1依據(jù)YY/T 0316的附錄E(表E.1)列舉了手術(shù)器械有關(guān)的可能危害示例的不完全清單,以幫助判定與手術(shù)器械有關(guān)的危害�。注冊(cè)申請(qǐng)人還應(yīng)根據(jù)自身產(chǎn)品特點(diǎn)確定其他可能危害。針對(duì)產(chǎn)品的各項(xiàng)風(fēng)險(xiǎn)��,注冊(cè)申請(qǐng)人應(yīng)采取控制措施�,確保風(fēng)險(xiǎn)降到可接受的程度。
2. 醫(yī)療器械安全和性能基本原則清單
本指導(dǎo)原則范圍內(nèi)的手術(shù)器械對(duì)醫(yī)療器械安全和性能基本原則清單的符合性見(jiàn)附錄2�����,注冊(cè)申請(qǐng)人可參考《醫(yī)療器械安全和性能基本原則》符合性技術(shù)指南編寫(xiě)該清單�。
3. 產(chǎn)品技術(shù)要求及檢驗(yàn)報(bào)告
3.1 申報(bào)產(chǎn)品適用標(biāo)準(zhǔn)情況
注冊(cè)申請(qǐng)人需列表說(shuō)明申報(bào)產(chǎn)品可參考的國(guó)家標(biāo)準(zhǔn)和行業(yè)標(biāo)準(zhǔn)����,可參考標(biāo)準(zhǔn)詳見(jiàn)附錄3。
產(chǎn)品適用的標(biāo)準(zhǔn)應(yīng)為現(xiàn)行有效版�,建議申請(qǐng)人主動(dòng)跟蹤相關(guān)標(biāo)準(zhǔn)的更新情況。
3.2 產(chǎn)品技術(shù)要求
產(chǎn)品技術(shù)要求需參照《醫(yī)療器械產(chǎn)品技術(shù)要求編寫(xiě)指導(dǎo)原則》等文件進(jìn)行編制�。
手術(shù)器械性能指標(biāo)可參考《手術(shù)電極注冊(cè)技術(shù)審查指導(dǎo)原則》及附錄3中適用標(biāo)準(zhǔn),結(jié)合產(chǎn)品特征制定�,可分為通用要求、專(zhuān)用要求�����、與系統(tǒng)配合的要求、電氣安全要求���、電磁兼容要求等�,詳見(jiàn)附錄4�����。
3.3檢驗(yàn)報(bào)告
同一注冊(cè)單元應(yīng)按產(chǎn)品風(fēng)險(xiǎn)與技術(shù)指標(biāo)的覆蓋性來(lái)選擇典型產(chǎn)品�����。不同的末端執(zhí)行器結(jié)構(gòu)(如鉗類(lèi)��、剪類(lèi)等)應(yīng)分別選取典型型號(hào)進(jìn)行性能指標(biāo)的檢測(cè)��。
典型產(chǎn)品應(yīng)能代表申請(qǐng)注冊(cè)產(chǎn)品的安全性和有效性���,一般選取結(jié)構(gòu)最復(fù)雜�����、功能最全���、技術(shù)指標(biāo)最全的型號(hào)作為典型產(chǎn)品����,并提供檢測(cè)典型性說(shuō)明��。結(jié)構(gòu)最復(fù)雜型號(hào)一般為工作長(zhǎng)度最長(zhǎng)型號(hào)�����。
手術(shù)器械與系統(tǒng)配合使用的功能��,應(yīng)根據(jù)產(chǎn)品的設(shè)計(jì)特性選擇典型型號(hào)進(jìn)行檢測(cè)����,通常應(yīng)選擇結(jié)構(gòu)最復(fù)雜�、自由度最多、末端執(zhí)行器位姿空間(角度�����、距離)最大的器械作為典型型號(hào)進(jìn)行檢測(cè)�����,不同的末端執(zhí)行器、傳動(dòng)方式(桿傳動(dòng)����、絲傳動(dòng))應(yīng)分別選取典型型號(hào)進(jìn)行檢測(cè)。配合使用功能應(yīng)參考YY/T 1712標(biāo)準(zhǔn)的要求�。
電氣安全,應(yīng)根據(jù)產(chǎn)品的設(shè)計(jì)特性選擇典型型號(hào)進(jìn)行檢測(cè)���,通常應(yīng)選擇結(jié)構(gòu)最復(fù)雜�、額定附件電壓最大的高頻手術(shù)器械作為典型型號(hào)���;單極手術(shù)器械���、雙極手術(shù)器械應(yīng)分別選取典型型號(hào)進(jìn)行檢測(cè);防電擊程度不同(如BF和CF型)的手術(shù)器械�����,應(yīng)分別選取典型型號(hào)進(jìn)行檢測(cè)�。手術(shù)器械配合高頻手術(shù)設(shè)備工作時(shí),使用的高頻輸出模式及參數(shù)不同的應(yīng)分別檢測(cè)����。
電磁兼容����,依據(jù)YY0505或YY9706.102�����、GB9706.4或GB9706.202以及YY9706.277標(biāo)準(zhǔn)的要求����,根據(jù)腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的配置,應(yīng)連接盡可能多的(至少包括單極和雙極手術(shù)器械各一個(gè))且結(jié)構(gòu)最復(fù)雜的手術(shù)器械�����,選擇長(zhǎng)度最長(zhǎng)的線纜�����,配置滿足腹腔內(nèi)窺鏡手術(shù)系統(tǒng)預(yù)期臨床使用各工作模式(包括:電切�����、電凝�����、氬離子凝等)的高頻手術(shù)設(shè)備���。發(fā)射和抗擾度試驗(yàn)的測(cè)試模式應(yīng)滿足附錄5的要求����。
如手術(shù)器械單獨(dú)進(jìn)行注冊(cè)�,應(yīng)配合可配合使用的腹腔內(nèi)窺鏡手術(shù)系統(tǒng)一起檢測(cè)。
4. 研究資料
根據(jù)申報(bào)手術(shù)器械的具體特點(diǎn)���,提供適用的研究資料�����。
4.1化學(xué)和物理性能研究
應(yīng)提供手術(shù)器械化學(xué)/材料表征及產(chǎn)品性能研究資料�����。提供化學(xué)/材料表征�、物理和/或機(jī)械性能指標(biāo)的確定依據(jù)����。
性能指標(biāo)應(yīng)全面��,綜合考慮手術(shù)器械的適用范圍���、技術(shù)特征、適用的法規(guī)標(biāo)準(zhǔn)及規(guī)范性文件的要求�����,包括手術(shù)器械本身的性能指標(biāo)����、與系統(tǒng)配合使用的性能指標(biāo),及器械與系統(tǒng)其他部分(如機(jī)械臂���、手術(shù)器械附件等)的配合性或兼容性性能指標(biāo)���。
4.2電氣系統(tǒng)安全性研究
應(yīng)提供電氣安全性及電磁兼容性的研究資料。
如高頻手術(shù)器械配合通用高頻手術(shù)設(shè)備使用�,應(yīng)選擇可配合的典型型號(hào)進(jìn)行檢測(cè),并提供典型性說(shuō)明��。
如腹腔內(nèi)窺鏡手術(shù)系統(tǒng)對(duì)高頻手術(shù)設(shè)備的控制功能包含設(shè)備廠家未公開(kāi)宣稱(chēng)的功能�����,如輸出參數(shù)設(shè)置等����,應(yīng)配合該設(shè)備進(jìn)行檢測(cè),并提交與設(shè)備制造商的聯(lián)合開(kāi)發(fā)協(xié)議�;僅通過(guò)腳踏開(kāi)關(guān)控制高頻手術(shù)設(shè)備能量輸出通常不需要聯(lián)合開(kāi)發(fā)協(xié)議,但應(yīng)對(duì)該功能進(jìn)行驗(yàn)證并提交相應(yīng)的驗(yàn)證資料�����。
電磁兼容檢測(cè)報(bào)告應(yīng)體現(xiàn)高頻手術(shù)設(shè)備的注冊(cè)人���、型號(hào)等信息�。列明高頻手術(shù)設(shè)備與手術(shù)器械之間的連接線纜信息��,如線纜長(zhǎng)度��、是否屏蔽�、制造商等。
4.3生物學(xué)特性研究
應(yīng)對(duì)成品中與患者直接或間接接觸的材料進(jìn)行生物學(xué)評(píng)價(jià)��。
手術(shù)器械與人體接觸的部件有器械頭端部��、桿部����。應(yīng)明確各器械或配合使用附件(如能量護(hù)套)與人體接觸材料的部件名稱(chēng)�����、材料名稱(chēng)等信息�����,提供圖示說(shuō)明與人體接觸材料對(duì)應(yīng)的位置����。同時(shí)應(yīng)考慮生產(chǎn)工藝及清潔滅菌對(duì)生物相容性的影響��,考慮設(shè)計(jì)生產(chǎn)過(guò)程中可能引入的污染物���、殘留物��、降解產(chǎn)物����、加工殘留物影響等���。
根據(jù)GB/T 16886.1的分類(lèi)要求����,手術(shù)器械及能量護(hù)套預(yù)期與人體組織短期接觸,屬于外部接入器械�。如需進(jìn)行生物學(xué)試驗(yàn)�,通常應(yīng)考慮細(xì)胞毒性、致敏�、皮內(nèi)反應(yīng)、材料介導(dǎo)的致熱性(有可浸提物/可瀝濾物器械適用)�����、急性全身毒性(有可浸提物/可瀝濾物器械適用)����。應(yīng)對(duì)生物學(xué)試驗(yàn)情況進(jìn)行概述。生物學(xué)試驗(yàn)可選取典型型號(hào)進(jìn)行����,通常應(yīng)選擇材料組成最復(fù)雜、表面積最大的型號(hào)作為典型型號(hào)���,并提供典型型號(hào)的選擇依據(jù)說(shuō)明�����。
生物學(xué)試驗(yàn)報(bào)告應(yīng)體現(xiàn)產(chǎn)品名稱(chēng)和型號(hào)�����,與申報(bào)產(chǎn)品對(duì)應(yīng)���。如使用其他產(chǎn)品的生物學(xué)試驗(yàn)報(bào)告�,應(yīng)就試驗(yàn)產(chǎn)品與申報(bào)產(chǎn)品的差異性(材料來(lái)源或技術(shù)規(guī)范��、產(chǎn)品配方/工藝/初包裝或滅菌��、運(yùn)輸貯存條件�����、預(yù)期用途��、不良生物反應(yīng)等)對(duì)生物相容性的影響進(jìn)行評(píng)價(jià)����,如評(píng)價(jià)資料不足以證明申報(bào)產(chǎn)品的生物相容性,應(yīng)重新開(kāi)展生物學(xué)評(píng)價(jià)�。
生物學(xué)試驗(yàn)應(yīng)在無(wú)菌的最終產(chǎn)品上、或取自最終產(chǎn)品上有代表性的樣品上、或與最終產(chǎn)品同樣方式加工(包括滅菌)的材料上進(jìn)行���。試驗(yàn)樣品應(yīng)根據(jù)申請(qǐng)人制定的清潔�、滅菌方法進(jìn)行處理�。
如手術(shù)器械的成分僅為醫(yī)用金屬材料(如醫(yī)用不銹鋼、醫(yī)用鈦合金等)����,不包含鍍層��,無(wú)加工助劑或者滅菌劑殘留�����,申請(qǐng)人如提供了材質(zhì)證明�����,明確材料名稱(chēng)���、化學(xué)成分及符合的標(biāo)準(zhǔn)���,可豁免生物學(xué)試驗(yàn)。
4.4清潔滅菌研究
手術(shù)器械有一次性使用和可重復(fù)使用兩種形式,在使用過(guò)程中與人體無(wú)菌組織接觸��,使用前應(yīng)進(jìn)行滅菌���。申請(qǐng)人應(yīng)開(kāi)展清潔�����、滅菌研究�����。
4.4.1生產(chǎn)企業(yè)滅菌
應(yīng)當(dāng)明確滅菌工藝(方法和參數(shù))和無(wú)菌保證水平(SAL)�����,并提供滅菌研究資料�。對(duì)于經(jīng)環(huán)氧乙烷滅菌的產(chǎn)品�,需明確產(chǎn)品的解析條件?�?蓞⒖肌稛o(wú)菌醫(yī)療器械滅菌工藝注冊(cè)技術(shù)審查指導(dǎo)原則》進(jìn)行相關(guān)注冊(cè)申報(bào)資料的準(zhǔn)備����。
滅菌研究可選擇典型型號(hào)進(jìn)行��,所選型號(hào)應(yīng)為滅菌挑戰(zhàn)性最強(qiáng)(如結(jié)構(gòu)最復(fù)雜)的型號(hào)����,且滅菌后應(yīng)對(duì)無(wú)菌性能進(jìn)行檢測(cè)����。
如申請(qǐng)人將申報(bào)產(chǎn)品加入已確認(rèn)的滅菌產(chǎn)品族,應(yīng)按照產(chǎn)品追加的要求���,將申報(bào)產(chǎn)品和已確認(rèn)產(chǎn)品或過(guò)程挑戰(zhàn)裝置影響滅菌效果的因素逐項(xiàng)比較�,如產(chǎn)品結(jié)構(gòu)特點(diǎn)�����、材料�����、無(wú)菌屏障系統(tǒng)或保護(hù)性包裝的方式����、生產(chǎn)工藝�����、初始污染菌水平、密度���、裝載方式等�,證明申報(bào)產(chǎn)品的滅菌挑戰(zhàn)性低于已確認(rèn)產(chǎn)品或過(guò)程挑戰(zhàn)裝置���。
如能量護(hù)套作為注冊(cè)單元的一部分進(jìn)行申報(bào)���,應(yīng)提交其滅菌研究資料。
4.4.2使用者滅菌
應(yīng)明確推薦的滅菌工藝(方法和參數(shù))��、所推薦滅菌工藝的確定依據(jù)�;對(duì)可重復(fù)使用產(chǎn)品,應(yīng)提供滅菌耐受性研究資料���。應(yīng)明確滅菌后測(cè)試的性能指標(biāo)及該指標(biāo)的選擇依據(jù)�����?���?蓞⒖肌犊芍貜?fù)使用醫(yī)療器械再處理說(shuō)明和確認(rèn)方法注冊(cè)技術(shù)審查指導(dǎo)原則》。
高頻連接線纜有可能進(jìn)入手術(shù)無(wú)菌區(qū)域��,基于使用風(fēng)險(xiǎn)應(yīng)進(jìn)行滅菌并提交滅菌研究資料�����。
所驗(yàn)證器械應(yīng)經(jīng)受最?lèi)毫拥奈⑸锾魬?zhàn)和滅菌挑戰(zhàn)����,應(yīng)考慮最復(fù)雜結(jié)構(gòu)、最不利的微生物負(fù)載水平和多次使用等情形的影響��。
4.4.3使用者清潔
對(duì)于終端用戶滅菌的手術(shù)器械�����,應(yīng)明確推薦的清潔工藝����、工藝的確定依據(jù)以及相關(guān)研究資料���。應(yīng)選擇最不易清潔的型號(hào)進(jìn)行���,考慮最難以清潔的污染物殘留情形��。清潔應(yīng)最大程度減少污染物在每次使用間的轉(zhuǎn)移�����,防止殘留物在器械使用壽命內(nèi)的積聚����。
4.4.4殘留毒性
若產(chǎn)品經(jīng)滅菌后可能產(chǎn)生殘留物質(zhì),應(yīng)當(dāng)對(duì)滅菌后的產(chǎn)品進(jìn)行殘留毒性的研究��,明確殘留物信息及采取的處理方法�,并提供相關(guān)研究資料。應(yīng)給出殘留物限值的確定依據(jù)�����。對(duì)于經(jīng)環(huán)氧乙烷滅菌的產(chǎn)品�����,需考慮的殘留毒性應(yīng)包括環(huán)氧乙烷和2-氯乙醇�。應(yīng)分析影響滅菌殘留的各種因素,如解析間溫度���、換氣次數(shù)��、產(chǎn)品本身的材料�、裝載方式等,考慮最易產(chǎn)生滅菌殘留的情形�����。
4.4.5以非無(wú)菌狀態(tài)交付的手術(shù)器械�����,應(yīng)當(dāng)提供證明包裝能減少產(chǎn)品受到微生物污染的風(fēng)險(xiǎn)��,且適用于注冊(cè)申請(qǐng)人規(guī)定滅菌方法的研究資料�����。
4.5動(dòng)物試驗(yàn)研究
腹腔內(nèi)窺鏡手術(shù)系統(tǒng)產(chǎn)品注冊(cè)時(shí)一般需進(jìn)行動(dòng)物試驗(yàn)���,動(dòng)物試驗(yàn)可用于為產(chǎn)品的設(shè)計(jì)定型提供證據(jù)���,證明器械的安全有效性,也可為產(chǎn)品能否用于人體研究提供支持�??蓞⒖肌夺t(yī)療器械動(dòng)物試驗(yàn)研究注冊(cè)審查指導(dǎo)原則 第一部分:決策原則》決定申報(bào)的手術(shù)器械是否需要開(kāi)展動(dòng)物試驗(yàn)研究�����,參考《醫(yī)療器械動(dòng)物試驗(yàn)研究注冊(cè)審查指導(dǎo)原則 第二部分:試驗(yàn)設(shè)計(jì)���、實(shí)施質(zhì)量保證》進(jìn)行動(dòng)物試驗(yàn)的設(shè)計(jì)和實(shí)施。
動(dòng)物試驗(yàn)研究應(yīng)確保能夠涵蓋預(yù)期的手術(shù)任務(wù)及不同類(lèi)型的組織��。預(yù)期的手術(shù)任務(wù)應(yīng)與手術(shù)器械的預(yù)期用途相匹配�,如抓取、牽拉��、剝離�����、切割����、凝血、持針�����、打結(jié)、縫合�、結(jié)扎等;組織類(lèi)型應(yīng)包括實(shí)質(zhì)器官(致密或精細(xì))�、中空器官(厚/密或薄/精細(xì))、結(jié)締組織(厚或?���。⒓∪饨M織或纖維組織等����。
如在已注冊(cè)腹腔內(nèi)窺鏡手術(shù)系統(tǒng)中申請(qǐng)注冊(cè)變更或增加手術(shù)器械型號(hào),應(yīng)評(píng)估新增型號(hào)與已注冊(cè)型號(hào)的差異���。如新增型號(hào)無(wú)等同的前代產(chǎn)品或在已注冊(cè)型號(hào)基礎(chǔ)上進(jìn)行設(shè)計(jì)變更����,如腕部結(jié)構(gòu)變更�、傳動(dòng)方式變更等,應(yīng)通過(guò)動(dòng)物試驗(yàn)證明新增型號(hào)能夠?qū)崿F(xiàn)預(yù)期功能并保證其安全性���。
動(dòng)物試驗(yàn)可選擇典型型號(hào)進(jìn)行�。典型型號(hào)取決于手術(shù)器械的結(jié)構(gòu)特征����、適用范圍及具體的變更情形���。
5. 穩(wěn)定性研究
5.1貨架有效期
對(duì)于無(wú)菌提供的手術(shù)器械應(yīng)提供貨架有效期和包裝研究資料����,可通過(guò)對(duì)產(chǎn)品和包裝進(jìn)行加速老化和/或?qū)崟r(shí)老化試驗(yàn)及運(yùn)輸試驗(yàn),試驗(yàn)后對(duì)產(chǎn)品進(jìn)行性能���、功能和無(wú)菌檢測(cè)���,對(duì)包裝外觀、完整性和無(wú)菌屏障系統(tǒng)的性能進(jìn)行驗(yàn)證�����,證明產(chǎn)品在貨架有效期內(nèi)保持無(wú)菌且性能功能符合預(yù)期要求����。加速老化和無(wú)菌屏障系統(tǒng)的性能驗(yàn)證可參考YY/T 0681系列標(biāo)準(zhǔn)。
5.2使用穩(wěn)定性/可靠性
對(duì)于有限次重復(fù)使用的手術(shù)器械應(yīng)明確使用次數(shù)�����,并提供使用穩(wěn)定性/可靠性研究資料。
應(yīng)說(shuō)明使用次數(shù)的記錄方式及如何避免超使用次數(shù)使用����。手術(shù)器械的使用穩(wěn)定性主要取決于重復(fù)使用引起的性能降低,其使用次數(shù)研究通常與滅菌耐受性研究合并進(jìn)行�。對(duì)手術(shù)器械模擬多次使用(如手術(shù)器械按照規(guī)定的適用范圍施加一定的夾持力、剪切力��,進(jìn)行縫合���、打結(jié)等操作����,高頻手術(shù)器械應(yīng)同時(shí)模擬能量輸出)��、清潔�、滅菌后,對(duì)產(chǎn)品性能和安全進(jìn)行驗(yàn)證�����,證明產(chǎn)品的性能功能滿足使用要求����。申請(qǐng)人應(yīng)明確驗(yàn)證的性能指標(biāo)及該指標(biāo)的選擇依據(jù)�。模擬實(shí)際使用時(shí)應(yīng)考慮使用過(guò)程中的最不利情形��,如夾持力最大�、輸出能量最高等。使用穩(wěn)定性應(yīng)模擬產(chǎn)品實(shí)際使用的工作條件����,且該條件應(yīng)與說(shuō)明書(shū)中規(guī)定的條件一致����。
可選擇典型型號(hào)進(jìn)行使用穩(wěn)定性/可靠性研究,并提交典型型號(hào)選擇依據(jù)��。工作原理不同的手術(shù)器械����,如單極手術(shù)器械和雙極手術(shù)器械,應(yīng)分別選取典型性型號(hào)�。結(jié)構(gòu)不同的手術(shù)器械,應(yīng)選擇結(jié)構(gòu)最復(fù)雜的作為典型性型號(hào)��。傳動(dòng)方式不同的手術(shù)器械�����,如桿傳動(dòng)和絲傳動(dòng),應(yīng)分別選取典型性型號(hào)���。
典型型號(hào)應(yīng)基于器械設(shè)計(jì)和預(yù)期用途����,通常為結(jié)構(gòu)最復(fù)雜�、故障率最高的器械。故障率一般取決于固有的設(shè)計(jì)載荷和預(yù)期的臨床使用周期����。設(shè)計(jì)載荷與手術(shù)器械在使用過(guò)程中所承受的應(yīng)力有關(guān),臨床使用周期與器械在預(yù)期臨床使用過(guò)程中經(jīng)歷的操作或運(yùn)動(dòng)次數(shù)有關(guān)��。如單極彎剪在單極手術(shù)器械中結(jié)構(gòu)較復(fù)雜�,設(shè)計(jì)載荷較高,頭端運(yùn)動(dòng)次數(shù)較多����,可作為單極手術(shù)器械的典型性型號(hào)。施夾鉗類(lèi)手術(shù)器械���,不同的施夾鉗結(jié)構(gòu)及臨床使用次數(shù)相似�,但小型施夾鉗設(shè)計(jì)載荷高于中型或大型��,所以小型施夾鉗可作為施夾鉗類(lèi)手術(shù)器械的典型性型號(hào)。
5.3運(yùn)輸穩(wěn)定性
應(yīng)當(dāng)提供運(yùn)輸穩(wěn)定性和包裝研究資料�����,證明注冊(cè)申請(qǐng)人規(guī)定的運(yùn)輸條件不會(huì)對(duì)手術(shù)器械的特性和性能�,包括完整性和清潔度,造成不利影響�����。手術(shù)器械的運(yùn)輸穩(wěn)定性可參考標(biāo)準(zhǔn)GB/ T 14710或GB/T 4857系列標(biāo)準(zhǔn)的要求進(jìn)行����,也可以參考相應(yīng)的國(guó)際標(biāo)準(zhǔn)���,運(yùn)輸貯存環(huán)境應(yīng)與申請(qǐng)人產(chǎn)品說(shuō)明書(shū)中規(guī)定的條件一致���。運(yùn)輸試驗(yàn)后的檢測(cè)項(xiàng)目,應(yīng)給出合理性說(shuō)明����。
6. 其他資料
6.1接觸力研究資料
應(yīng)對(duì)手術(shù)器械與組織的接觸力過(guò)大造成的風(fēng)險(xiǎn)進(jìn)行分析,說(shuō)明相應(yīng)的控制措施��,并提交接觸力研究資料。
6.2 末端振動(dòng)研究資料
手術(shù)器械末端受力�、機(jī)械臂各關(guān)節(jié)電機(jī)振動(dòng)等多種原因均可引起器械末端振動(dòng),從而影響手術(shù)質(zhì)量���,甚至帶來(lái)不可接受的風(fēng)險(xiǎn)���,應(yīng)對(duì)手術(shù)器械末端振動(dòng)情況進(jìn)行研究。
可選擇典型型號(hào)進(jìn)行研究���,所選擇的典型型號(hào)應(yīng)能覆蓋其他器械的振動(dòng)情況�,代表器械運(yùn)動(dòng)的最不利情形�����,如器械運(yùn)動(dòng)范圍最大��。
如手術(shù)器械作為腹腔內(nèi)窺鏡手術(shù)系統(tǒng)的一部分進(jìn)行注冊(cè)�����,可合并機(jī)械臂的振動(dòng)研究一起進(jìn)行��,如單獨(dú)注冊(cè)�,應(yīng)提交手術(shù)器械的振動(dòng)研究資料��。全面分析振動(dòng)產(chǎn)生的原因(如輸入端����、輸出端�����、主從控制等)及需要采取的控制措施��,說(shuō)明振動(dòng)范圍�,分析振動(dòng)是否對(duì)器械操作及手術(shù)效果產(chǎn)生不利影響。應(yīng)說(shuō)明試驗(yàn)過(guò)程及振動(dòng)測(cè)試方法��,并對(duì)試驗(yàn)結(jié)果進(jìn)行分析得出結(jié)論���。
6.3耐高溫性能研究
為避免單極手術(shù)器械使用過(guò)程中對(duì)非目標(biāo)組織造成的損傷,一般使用能量護(hù)套進(jìn)行保護(hù)����。為驗(yàn)證能量護(hù)套對(duì)非目標(biāo)組織的保護(hù)效果,應(yīng)對(duì)其絕緣和耐高溫性能進(jìn)行研究��,提交相應(yīng)的研究資料��。
6.4 氣密性研究
手術(shù)器械的氣密性對(duì)于維持腹腔壓力,保證手術(shù)視野及可操作空間具有重要的作用��,應(yīng)對(duì)氣密性進(jìn)行研究��,提交手術(shù)器械氣密性研究資料�����。
申請(qǐng)人應(yīng)給出器械的氣密性指標(biāo)�����,說(shuō)明保持氣密性的方法�����,并提交相應(yīng)的研究資料�。
(四)臨床評(píng)價(jià)資料
本指導(dǎo)原則所指手術(shù)器械不屬于《免于進(jìn)行臨床評(píng)價(jià)目錄》中的產(chǎn)品,應(yīng)按照同品種對(duì)比或臨床試驗(yàn)方式進(jìn)行評(píng)價(jià)��。
(五)產(chǎn)品說(shuō)明書(shū)和標(biāo)簽樣稿
手術(shù)器械的說(shuō)明書(shū)���、標(biāo)簽樣稿應(yīng)當(dāng)符合《醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定》《手術(shù)電極注冊(cè)技術(shù)審查指導(dǎo)原則》及其他適用標(biāo)準(zhǔn)中有關(guān)說(shuō)明書(shū)和標(biāo)簽的要求的規(guī)定��,應(yīng)包括使用期限��、說(shuō)明書(shū)修訂或編制日期等細(xì)節(jié)����。
申請(qǐng)人還應(yīng)在手術(shù)器械說(shuō)明書(shū)中包含以下內(nèi)容:
1. 明確手術(shù)器械的清潔滅菌方式及滅菌參數(shù),并與研究資料一致�。如采用H2O2,甲醛滅菌,應(yīng)提供滅菌設(shè)備的制造商�����、型號(hào)信息����。
2.如手術(shù)器械預(yù)期與通用高頻手術(shù)設(shè)備配合使用,說(shuō)明書(shū)中應(yīng)給出配合使用高頻手術(shù)設(shè)備產(chǎn)品信息�����。鼓勵(lì)給出電磁兼容配合檢測(cè)的高頻手術(shù)設(shè)備的制造商����、型號(hào)等信息�。
專(zhuān)用的要求
3. 若手術(shù)器械為有限次使用,說(shuō)明書(shū)中應(yīng)明確使用次數(shù),并提示不能繼續(xù)使用的情形�。一次性使用的手術(shù)器械應(yīng)明確貨架有效期。
4. 應(yīng)說(shuō)明手術(shù)器械的安裝�����、拆卸���、更換方式�����。
5. 持針鉗類(lèi)器械的說(shuō)明書(shū)應(yīng)包括對(duì)可與該持針鉗配合使用附件的明確說(shuō)明����,若縫合針的結(jié)構(gòu)特殊��,需配合特定持針鉗使用���,可在說(shuō)明書(shū)內(nèi)說(shuō)明�。
6. 使用說(shuō)明應(yīng)包含在發(fā)生以下情況時(shí)�����,操作者快速安全地從患者身上移除手術(shù)器械所必需的信息:
- 腹腔內(nèi)窺鏡手術(shù)系統(tǒng)故障;
- 電源故障���;
- 緊急停止���;
- 操作者的決策。
7. 應(yīng)說(shuō)明手術(shù)器械末端振動(dòng)的位移和時(shí)間����。
(六)質(zhì)量管理體系文件
1.應(yīng)依據(jù)121號(hào)公告要求提供質(zhì)量管理體系核查文件。
2.若產(chǎn)品有多個(gè)研制�����、生產(chǎn)場(chǎng)地�,應(yīng)概述每個(gè)研制、生產(chǎn)場(chǎng)地的實(shí)際情況�����。
三��、參考文獻(xiàn)
[1] GB/T 16886.1���,醫(yī)療器械生物學(xué)評(píng)價(jià) 第1部分:風(fēng)險(xiǎn)管理過(guò)程中的評(píng)價(jià)與試驗(yàn)[S].
[2] YY/T 0316,醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用[S].
[3] 醫(yī)療器械監(jiān)督管理?xiàng)l例[Z].
[4] 國(guó)家市場(chǎng)監(jiān)管總局.醫(yī)療器械注冊(cè)與備案管理辦法(總局令第47號(hào))[Z],2021.8
[5] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械說(shuō)明書(shū)和標(biāo)簽管理規(guī)定(總局令第6號(hào))[Z]���,2014.6
[6] 國(guó)家藥品監(jiān)督管理局.關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告(2021年第121號(hào)公告)[Z]���,2021.9
[7] 原國(guó)家食品藥品監(jiān)督管理總局.醫(yī)療器械通用名稱(chēng)命名規(guī)則(總局令第19號(hào))[Z],2015.12.
[8] 原國(guó)家食品藥品監(jiān)督管理總局.總局關(guān)于發(fā)布醫(yī)療器械分類(lèi)目錄的公告(2017年第104號(hào)公告)[Z],2017.9
[9] 原國(guó)家食品藥品監(jiān)督管理總局.高頻手術(shù)設(shè)備注冊(cè)技術(shù)審查指導(dǎo)原則 ( 2016年第21號(hào)通告)[Z].,2016.4
[10] 原國(guó)家食品藥品監(jiān)督管理總局.手術(shù)電極注冊(cè)技術(shù)審查指導(dǎo)原則(2017年修訂版)(2017年第41號(hào)通告)[Z],2016.4
[11] 國(guó)家藥品監(jiān)督管理局.醫(yī)療器械動(dòng)物試驗(yàn)研究注冊(cè)審查指導(dǎo)原則 第一部分:決策原則(2021年修訂版)(2021年第75號(hào)通告)[Z], 2021.9
[12] 國(guó)家藥品監(jiān)督管理局. 關(guān)于發(fā)布醫(yī)療器械產(chǎn)品技術(shù)要求編寫(xiě)指導(dǎo)原則的通告(2022年第8號(hào)) [Z],2022.2
[13] 國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心. 關(guān)于發(fā)布醫(yī)療器械安全和性能基本原則符合性技術(shù)指南的通告(2022年第29號(hào))[Z],2022.7�����。
[14] 國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心. 無(wú)菌醫(yī)療器械滅菌工藝注冊(cè)審查指導(dǎo)原則.
[15] 國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心. 可重復(fù)使用醫(yī)療器械再處理說(shuō)明和確認(rèn)方法注冊(cè)審查指導(dǎo)原則.
[16] GB/ T 14710���,醫(yī)用電器環(huán)境要求及試驗(yàn)方法[S].
[17] GB/T 4857��,包裝 運(yùn)輸包裝件系列標(biāo)準(zhǔn)[S].
[18] YY/T 0681�����,無(wú)菌醫(yī)療器械包裝試驗(yàn)方法 系列標(biāo)準(zhǔn)[S].
[19] IEC 60068-2: Environmental testing[S]
[20] YY/T 1268�,環(huán)氧乙烷滅菌的產(chǎn)品追加和過(guò)程等效[S]
四��、起草單位
國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心